Wat als kanker zou kunnen worden aangezet om zichzelf te vernietigen tumoren? Wetenschappers van het MIT hebben een innovatieve strategie ontwikkeld die de tumorcellen zelf tot bondgenoten van het immuunsysteem maakt. In plaats van de tumor van buitenaf aan te vallen, doet deze experimentele therapie dat van binnenuit, door de ‘zelfvernietigingsknop’ te activeren en het effect van de huidige immuuntherapieën te versterken.
Door kankercellen te stimuleren om een molecuul te produceren dat een signaalroute in nabijgelegen immuuncellen activeert, hebben onderzoekers van het MIT (Verenigde Staten) een manier gevonden om tumoren te dwingen hun eigen vernietiging in gang te zetten.
EEN WEG DIE DE TUMOR TOT ZIJN EIGEN VIJAND MAAKT
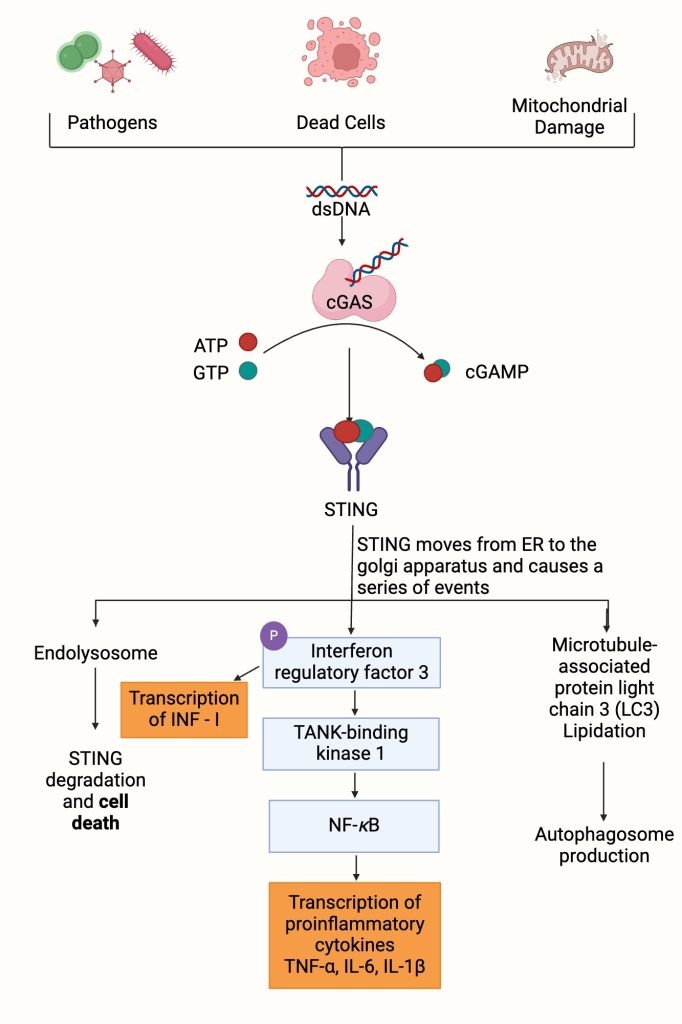
De activering van deze signaalroute, bekend als de cGAS-STING-route, bleek nog effectiever in combinatie met bestaande immuuntherapeutische geneesmiddelen, bekend als checkpointremmers, in een studie met muizen. Deze gecombineerde behandeling slaagde erin de tumorgroei onder controle te houden.
De onderzoekers activeerden de cGAS-STING-route in immuuncellen door middel van boodschapper-RNA dat aan kankercellen werd toegediend. Deze methode zou de bijwerkingen van het toedienen van hoge doses van een STING-activator kunnen voorkomen en maakt gebruik van een natuurlijk proces in het lichaam. Volgens de onderzoekers zou dit de ontwikkeling van een behandeling voor patiënten vergemakkelijken.
“Onze aanpak maakt gebruik van het eigen mechanisme van de tumor om immuunstimulerende moleculen te produceren, waardoor een krachtige antitumorrespons ontstaat”, legt Natalie Artzi uit, hoofdonderzoeker aan het MIT Institute for Medical Engineering and Science, universitair hoofddocent geneeskunde aan de Harvard Medical School, lid van de kernfaculteit van het Wyss Institute for Biologically Inspired Engineering van Harvard en hoofdauteur van de studie.
“Door de cGAS-niveaus in kankercellen te verhogen, kunnen we de effectiviteit van de toediening verbeteren – in vergelijking met het richten op immuuncellen, die schaarser zijn in de tumoromgeving – en de natuurlijke productie van cGAMP stimuleren, wat op zijn beurt de immuuncellen lokaal activeert”, legt ze uit. “Deze strategie versterkt niet alleen de antitumorale immuniteit, maar vermindert ook de toxiciteit die gepaard gaat met de directe toediening van STING-agonisten, waardoor we dichter bij veiligere en effectievere immuuntherapieën tegen kanker komen.”
VEELBELOVENDE RESULTATEN IN DIERMODELLEN

Aan de hand van een melanoommodel bij muizen hebben de onderzoekers het potentieel van hun nieuwe strategie voor het elimineren van kankercellen geëvalueerd. Ze injecteerden mRNA dat cGAS codeert, ingekapseld in lipide-nanodeeltjes, in de tumoren. Een groep muizen kreeg alleen deze behandeling, een andere groep kreeg een immuuncontrolepuntremmer en een derde groep kreeg beide behandelingen.
Afzonderlijk toegediend remden zowel cGAS als de immuuncontrole-remmer de tumorgroei aanzienlijk. De beste resultaten werden echter waargenomen bij de muizen die beide behandelingen kregen. In deze groep werden de tumoren bij 30% van de muizen volledig uitgeroeid, terwijl in de groepen die slechts één behandeling kregen, geen enkele tumor volledig werd verwijderd.
Uit een analyse van de immuunrespons bleek dat de behandeling met mRNA de productie van interferon stimuleerde, evenals die van vele andere immuunsignaleringsmoleculen die verschillende immuuncellen activeerden, waaronder macrofagen en dendritische cellen. Deze cellen helpen bij het stimuleren van T-cellen, die vervolgens kankercellen kunnen vernietigen.
De onderzoekers slaagden erin deze reacties op te wekken met slechts een kleine dosis cGAMP geproduceerd door kankercellen, wat zou kunnen helpen om een van de mogelijke obstakels voor het gebruik van cGAMP als therapie te overwinnen: er zijn hoge doses nodig om een immuunrespons te stimuleren, en deze doses kunnen algemene ontstekingen, weefselschade en auto-immuunreacties veroorzaken.
Wanneer cGAMP alleen wordt geïnjecteerd, verspreidt het zich door het lichaam en wordt het snel uit de tumor verwijderd, terwijl in deze studie de mRNA-nanodeeltjes en cGAMP op de plaats van de tumor bleven.
“De bijwerkingen van dit soort moleculen kunnen behoorlijk ernstig zijn, en een van de potentiële voordelen van onze aanpak is dat bepaalde toxiciteit die zou kunnen optreden bij toediening van vrije moleculen, mogelijk kan worden tegengegaan”, zegt Cryer.
VOLGENDE STAPPEN: NAAR EEN BREDER TOEPASSINGSGEBIED
De onderzoekers hopen nu het toedieningssysteem aan te passen zodat het via een systemische injectie kan worden toegediend, in plaats van rechtstreeks in de tumor. Ze zijn ook van plan om de mRNA-therapie te testen in combinatie met chemotherapie of radiotherapie die het DNA beschadigen, wat de effectiviteit ervan zou kunnen verhogen doordat er meer dubbelstrengs DNA beschikbaar is om de synthese van cGAMP te activeren.